В поддержании гомеостаза биологических систем высшего уровня участвуют механизмы гомеостаза биосистем низкого уровня. Поэтому для понимания функционирования биологических систем разных уровней необходимо сначала ознакомиться с механизмами адаптации на молекулярном и клеточном уровнях организации живого.
Прежде всего сохранение эффективности функционирования биологических систем при изменении условий существования обеспечивается поддержкой гомеостаза на молекулярном уровне. Можно выделить три главных направления развития таких процессов.
Направления адаптации на молекулярном уровне организации живого:

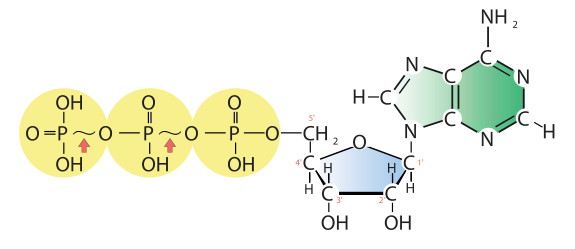
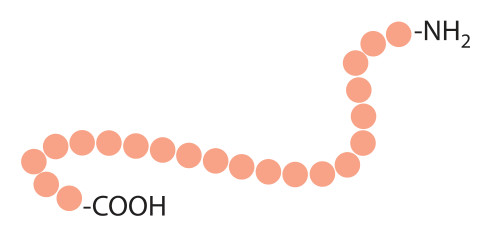
Одним из направлений является сохранение структурной целостности и функциональной активности макромолекул (нуклеиновых кислот, ферментов, структурных и сократительных белков) и надмолекулярных комплексов (хроматина, рибосом, мембран).
Приведем несколько примеров. Репарация ДНК приводит к восстановлению структуры этой молекулы в случае повреждений, вызванных действием негативных факторов (ионизирующее излучение, яды и т.п.) или же спонтанных ошибок (например, во время репликации).
Специализированные белковые комплексы, которые называют протеасомы, контролируют состояние важных внутриклеточных белков и разрушают старые или поврежденные. Разрушение старых или поврежденных клеточных структур также осуществляется с помощью пищеварительных ферментов, которые содержатся в лизосомах. Указанный процесс называют аутофагия.
Неправильное течение перечисленных процессов может быть причиной возникновения мутаций или приводить к развитию заболеваний.
Не менее важным является обеспечение клеток организмов соединениями, необходимыми для синтеза собственных макромолекул и для получения энергии. В случае поступления избыточных энергетических соединений, они могут превращаться в резервные вещества (вспомните известные вам резервные углеводы растительных и животных клеток). В случае дополнительной потребности в энергии резервные вещества расщепляются. Внутри клеток поддерживается относительно постоянная концентрация таких соединений. Например, при физиологических условиях количество АТФ колеблется более чем на 10%.
В-третьих, существуют многочисленные адаптации, направленные на регуляцию обмена веществ, которые адекватно подстраивает функционирования клеток к изменениям в окружающей среде. Многим биохимическим реакциям присуща способность к саморегуляции. В частности, уровень активности ферментов часто определяется концентрацией продуктов реакции. Обычно они тормозят работу фермента: в результате накопления продуктов реакции скорость реакции снижается, а следовательно образования этих веществ прекращается. Таким образом исключается избыточное накопление создаваемых соединений. Некоторые реакции гликолиза интенсифицируются вследствие увеличения концентрации АМФ, является следствием расщепления молекул АТФ и снижение энергетических запасов клетки. Увеличение скорости гликолиза сопровождается увеличением количества синтезированных молекул АТФ, поэтому энергетический баланс восстанавливается.
Известны и другие способы регуляции ферментативных реакций.
Функционирование некоторых ферментов зависит от наличия дополнительных — веществ небелковой природы — коферментов. Ими могут быть, в частности, производные витаминов. Другим путем регуляции работы ферментов является присоединение к ним определенных соединений, например остатка ортофосфорной кислота. Такую реакцию называют фосфорилированием. В результате нее неактивный фермент становится активным и начинает выполнять свою функцию. Фосфорилирование может вызвать и обратный эффект — измененный белок переходит из активного состояния в неактивное. Такие изменения могут происходить внутри клеток вследствие воздействия на них различных раздражителей — гормонов, медиаторов и тому подобное. Некоторые вещества могут блокировать активный центр фермента — это приводит к нарушению его функционирования. Таким образом, изменение активности фермента является одним из способов регуляции функционирования клеток на молекулярном уровне.
Фосфорилирование — процесс переноса остатка фосфорной кислоты от фосфорилирующего агента-донора к субстрату, как правило, катализируемый ферментами и ведущий к образованию сложных эфиров фосфорной кислоты: АТФ + R-OH → АДФ + R-OPO3H.
Синтез и накопление определенных соединений может быть непосредственным адаптационным фактором. Например, увеличение концентрации растворенных соединений в воде снижает температуру ее замерзания, обеспечивающий функционирование макромолекул при низкой температуре. Так, в клетках растений для выдерживания низких температур накапливаются углеводы и масла, а в клетках членистоногих — глицерин.
Перечисленные три направления адаптации не являются взаимоисключающими, некоторые реакции гомеостаза могут включать элементы нескольких из них.
Генетические основы формирования адаптаций
Часто изменения функционирования макромолекул связаны с регуляцией активности генов, с механизмами которой вы познакомились ранее (статьи Адаптация в биологии и Адаптация как свойство биологических систем). Для примера рассмотрим потребление кишечной палочкой углеводов. Обычным источником энергии для нее это молекулы глюкозы. Однако при ее недостатке бактерия способна расщеплять другой углевод — лактозу. Это обеспечивается определенными ферментами, которые кодируются соответствующими генами. Рядом с ними в молекуле ДНК расположены две важные регуляторные участки: промотор и оператор. Промотор является местом связывания РНК-полимеразы, которая осуществляет транскрипцию. Однако контакту РНК-полимеразы с молекулой ДНК может препятствовать белок-репрессор, который связывается с оператором. Важной особенностью работы этой системы является то, что наличие в цитоплазме лактозы приводит к отсоединению репрессора от молекулы ДНК. Тогда РНК-полимераза получает доступ к промотору и инициирует транскрипцию. В результате в клетке синтезируются ферменты, необходимые для расщепления лактозы. Адаптационный смысл описанного механизма в том, что при отсутствии лактозы эти гены неактивны, а клетка экономит ресурсы на синтезе соответствующих (ненужных) белков.
Изменения в функционировании генетического аппарата сопровождают не только индивидуальные приспособления организмов к условиям существования, но и эволюционные процессы. Современная биология имеет мощные инструменты для анализа изменений, происходящих с генотипами различных организмов в процессе исторического развития. В организмов разных групп было найдено гены, имеющие подобную структуру, а их белковые продукты выполняют схожие функции. В процессе эволюции гены могут приобретать изменений вследствие мутаций, а те, что обеспечивают лучшую приспособленность организмов, закрепляются в генофонде популяций. Некоторые гены могут удваиваться с последующей дивергенцией строения и функций. Такое увеличение количества генов создает дополнительный материал для естественного отбора. Другие же могут терять свою функцию, превращаясь в нерабочие псевдогены. Ярким примером является эволюция рецепторов в зрительной и слуховой сенсорных системах у наземных позвоночных.
Итак, молекулярные механизмы адаптации имеют важное значение в приспособлении организмов и являются основой клеточного уровня адаптации.
Адаптации на клеточном уровне
Процессы на молекулярном уровне организации живого является основой всех адаптационных процессов. На их основе формируются более сложные реакции с перестройкой жизнедеятельности и структуры клеток, изменением характера их взаимодействий, что приводит к адаптивным сдвигам деятельности органов и их систем. Можно выделить несколько направлений клеточного ответа на внешние воздействия.
Адаптационные изменения объема клетки. При определенных типах воздействий может происходить существенное уменьшение объема клетки — атрофия. В случае, если таких клеток много, может изменяться объем и функционирования органа, образованный этими клетками. Известным эффектом является атрофия скелетных мышц, вызванная снижением их активности вследствие травм (повреждения нервов) или существенного снижения двигательной активности.
Адаптивность этой реакции состоит в том, что организм тратит меньше ресурсов на поддержание жизнедеятельности органа, который не используется. Подобный эффект присущ и сердечной мышце. Для того, чтобы предотвратить снижение объема и массы мышц, необходимо поддерживать минимальный объем ежедневной физической активности. Атрофия может быть физиологической, например, важный иммунный орган нашего организма тимус приобретает максимальную массу на первом году жизни, а в дальнейшем постепенно снижает ее. Гипертрофия — процесс, который характеризуется увеличением объема клетки. Иногда это может свидетельствовать о нарушении функционирования органа.
Кроме этого, гипертрофия является главным путем увеличения объема органов, клетки которых способны к делению. Так, гипертрофия клеток печени делает возможным восстановление функциональности этого органа после гибели части клеток, например вследствие перенесенного вирусного гепатита.
Разделение, рост и гибель клеток как адаптивный фактор
Гиперплазия является способом увеличения массы органов вследствие деления клеток, при этом их объем, в отличие от гипертрофии, остается на стабильном уровне. Так происходит восстановление утраченных клеток, в том числе и физиологическое, например в многослойном ороговевающем эпителии. Увеличение объема молочных желез у млекопитающих в период беременности является адаптацией к будущему вскармливания малышей. Признаком нормальной гиперплазии является контролируемость этого процесса регуляторными факторами, например факторами роста. Состояние, когда вновь образованные клетки не реагируют на них и начинают никак не контролируемо делиться, называют неоплазией. Одним из его проявлений является формирование злокачественных опухолей при онкологических заболеваниях.
Адаптивным может быть не только клеточное деление или рост, но и прекращение роста или гибель клеток. Программируемую гибель клетки называют апоптозом. Этот процесс необходим для исчезновения временных органов (хвост у головастиков лягушек), контролируемого разрушения некоторых структур (опадение листьев растений осенью), влияния Т-лимфоцитов на чужеродные клетки, физиологического уничтожения старых клеток и тому подобное.
Еще одним путем клеточных адаптации является метаплазия, что представляет собой преобразование дифференцированных клеток в клетки другого типа в ответ на стрессовые факторы. Примером может быть замена нормального реснитчатого эпителия дыхательных путей на многослойный ороговевающий у курильщиков как ответ на длительное действие табачного дыма.
