Строение твердого вещества определяется не только взаимным расположением атомов внутри химических частиц, но и размещением самих частиц в пространстве относительно друг друга и расстояниями между ними. В зависимости от расположения частиц в пространстве различают ближний и дальний порядок.
Ближний порядок заключается в том, что частицы вещества закономерно размещаются в пространстве на определенных расстояниях и направлениях друг от друга. Если такая упорядоченность сохраняется или периодически повторяется во всем объеме твердого вещества, то формируется дальний порядок. Иначе говоря, дальний и ближний порядки — это наличие корреляции микроструктуры вещества либо в пределах всего макроскопического образца (дальний), либо в области с ограниченным радиусом (ближний). В зависимости от совокупного (или подавляющего) действия ближнего или дальнего порядка размещения частиц твердое тело может иметь кристаллическое или аморфное состояние.
Наиболее упорядоченным является размещение частиц в кристаллах (от греческого « кристалос » — лед), в которых атомы, молекулы или ионы расположены только в определенных точках пространства, названных узлами кристаллической решетки.
Кристаллическое состояние — это упорядоченная периодическая структура, которая характеризуется наличием как ближнего, так и дальнего порядка размещения частиц твердого вещества.
Характерным признаком кристаллических веществ по сравнению с аморфными является анизотропия.
Анизотропия — это разница физико-химических свойств кристаллического вещества (электро- и теплопроводности, прочности, оптических характеристик и т.д.) в зависимости от выбранного направления в кристалле .
Анизотропия обусловлена внутренним строением кристаллов. В разных направлениях расстояние между частицами в кристалле разная, поэтому и количественная характеристика того или иного свойства для этих направлений будет разной.
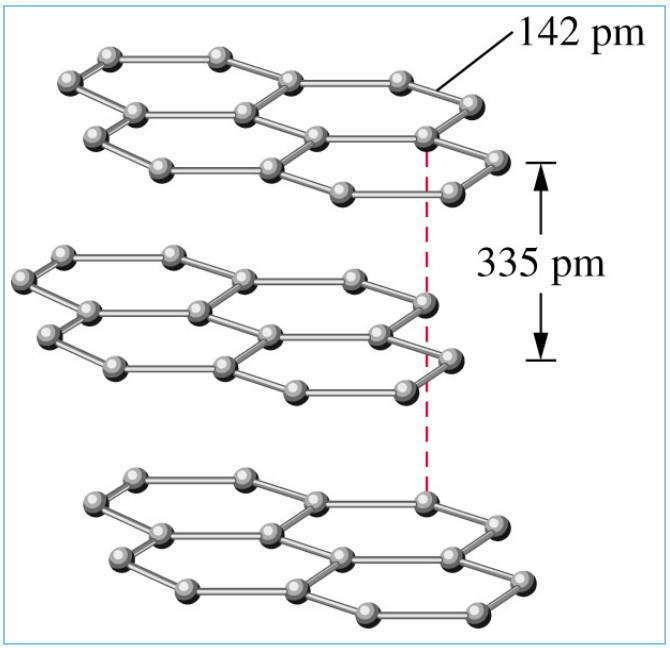
Особенно ярко анизотропия проявляется в монокристаллах. На этом свойстве основано производство лазеров, обработка монокристаллов полупроводников, изготовление кварцевых резонаторов и ультразвуковых генераторов. Типичным примером анизотропного кристаллического вещества является графит, структура которого представляет собой параллельные слои с различными энергиями связи в середине слоев и между отдельными слоями. Благодаря этому теплопроводность вдоль слоев в пять раз выше, чем в перпендикулярном направлении, а электропроводность в направлении отдельного слоя близка к металлической и сотни раз больше электропроводности в перпендикулярном направлении.
Иногда одно и то же вещество может образовывать кристаллы различной формы. Это явление называют полиморфизмом, а различные кристаллические формы одного вещества — полиморфными модификациями, например, алотропы алмаз и графит; a-, b-, g- и d-железо; a- и b-кварц (обратите внимание на различие понятий «аллотропия», которое относится исключительно к простым веществам в любом агрегатном состоянии, и «полиморфизм», которое характеризует строение только кристаллических соединений).
В то же время различные по составу вещества могут образовывать кристаллы одинаковой формы — это явление называют изоморфизмом. Так, изоморфными веществами, имеющими одинаковые кристаллические решетки, являются металлы Al и Cr и их оксиды; Ag и Au; BaCl2 и SrCl2 ; KMnO4 и BaSO4.
Подавляющее большинство твердых веществ при обычных условиях существует в кристаллическом состоянии.
Твердые вещества, не имеющие периодической структуры, относятся к аморфным (от греческого « аморфос» — бесформенный). Однако некоторая упорядоченность структуры в них присутствует. Она проявляется в закономерном размещении вокруг каждой частицы ее ближних «соседей», то есть аморфные вещества имеют только ближний порядок и этим напоминают жидкости, поэтому их с некоторым приближением можно рассматривать как переохлажденные жидкости с очень высокой вязкостью. Разница между жидким и твердым аморфным состоянием определяется характером теплового движения частиц: в аморфном состоянии они способны лишь к колебательным и вращательным движения, но не могут перемещаться в толще вещества.
Аморфное состояние — это твердое состояние вещества, характеризующееся наличием ближнего порядка в размещении частиц, а также изотропностью — одинаковыми свойствами в любом направлении.
Аморфное состояние веществ менее стабильно по сравнению с кристаллическим, так аморфные вещества могут переходить в кристаллическое состояние под действием механических нагрузок или при изменении температуры. Однако некоторые вещества могут находиться в аморфном состоянии в течение достаточно большого периода. Например, вулканическое стекло (возраст которого доходит до нескольких миллионов лет), обычное стекло, смолы, воск, большинство гидроксидов переходных металлов и тому подобное. При определенных условиях в аморфном состоянии могут находиться почти все вещества, кроме металлов и некоторых ионных соединений. С другой стороны, известны вещества, способные существовать только в аморфном состоянии (органические полимеры с неравномерной последовательностью элементарных звеньев).
Физические и химические свойства вещества в аморфном состоянии могут существенно отличаться от ее свойств в кристаллическом состоянии. Реакционная способность веществ в аморфном состоянии значительно выше, чем в кристаллическом. Например, аморфный GeO2 значительно активнее в химическом отношении, чем кристаллический.
Переход твердых веществ в жидкое состояние в зависимости от строения имеет свои особенности. Для кристаллического вещества плавления происходит при определенной температуре, которая является фиксированной для данного вещества, и сопровождается скачкообразным изменением ее свойств (плотность, вязкость и т.д.). Аморфные вещества, напротив, переходят в жидкое состояние постепенно, в течение некоторого интервала температур (так называемый интервал размягчения ), во время которого происходит плавное, медленное изменение свойств.
Сравнительная характеристика аморфных и кристаллических веществ:
| состояние
твердого вещества |
характеристика |
примеры |
| аморфное | 1. Ближний порядок размещения частиц;
2. Изотропность физических свойств; 3. Отсутствие фиксированной температуры плавления; 4. Термодинамическая нестабильность (большой запас внутренней энергии) 5. Текучесть |
Янтарь, стекло, органические полимеры |
| кристаллическое | 1. Дальний порядок размещения частиц;
2. Анизотропнисть физических свойств; 3. Фиксированная температура плавления; 4. Термодинамическая устойчивость (небольшой запас внутренней энергии) 5. Наличие элементов симметрии |
Металлы, сплавы, твердые соли, углерод (алмаз, графит). |
