Свойства твердого тела зависят от электронной структуры и особенностей взаимодействия всех его электронов и ядер, для описания которых на основе квантово-механических представлений Ф.Вильсоном (1931 г.) была предложена зонная теория твердого тела. Несмотря на то, что зонная теория справедлива только к идеальным или почти идеальным кристаллам, она считается удобной, наглядной, хотя и несколько приблизительной моделью, описывающей свойства твердого состояния веществ.
Зонная теория — это метод молекулярных орбиталей (МО), распространенный на ансамбль частиц, соединенных в кристалле.
При образовании кристаллов из изолированных атомов происходит перекрытие близких по энергии атомных орбиталей, и образование молекулярных орбиталей, количество которых равно общему количеству выходных атомных орбиталей, перекрываются. При росте числа взаимодействующих атомов в кристалле увеличивается число разрешенных молекулярных энергетических уровней, а энергетический порог между ними уменьшается. Благодаря этому создается непрерывная энергетическая зона, в которой переход электрона из низшего энергетического уровня на более высокий не требует больших затрат энергии.
Согласно методу МО взаимодействие атомов приводит к возникновению связующих и разрыхляющих молекулярных орбиталей, то есть атомные энергетические состояния расщепляются на молекулярные. Уже при взаимодействии двух одинаковых атомов дискретные атомные энергетические уровни превращаются в одну связующую и одну разрыхляющую орбиталь, причем энергия связующей орбитали меньше, а энергия разрыхляющей орбитали больше, чем энергия орбиталей изолированного атома. В системе, состоящей из 1 моль атомов, каждое атомное энергетический состояние расщепляется на NA молекулярных состояний (NA = 6,02 × 1023), поскольку образуется NA молекулярных орбиталей. Благодаря очень большому числу соседних молекулярных орбиталей, которые энергетически близки друг к другу, изменение энергии электронов на NA молекулярных орбиталях представляет собой непрерывную полосу энергетических уровней — зону.
Энергетическая зона — это совокупность большого количества очень близких по энергии дискретных энергетических уровней.
Общая ширина энергетической зоны, определяется разницей между самым низким и самым высоким уровнями, которая не зависит от количества атомов, а обусловлена равновесным расстоянием между атомами в кристалле.
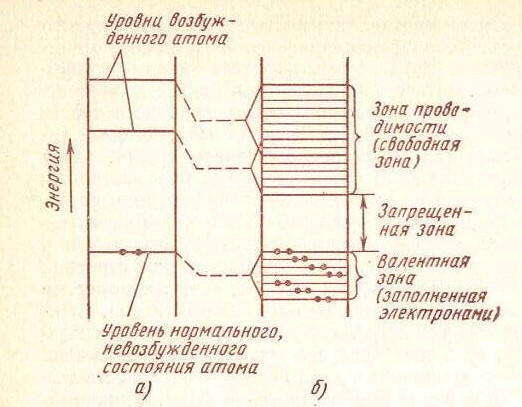
Энергетические уровни, на которых содержатся валентные электроны, образуют валентную зону. Свободные энергетические уровни, расположенные энергетически выше валентной зоны (а в некоторых случаях и в ее пределах), формируют зону проводимости. В зависимости от природы атомов и типа кристаллической решетки валентная зона и зона проводимости могут перекрывать или не перекрывать друг друга. В последнем случае между ними возникает разрыв — зона запрета.
В зависимости от типа атомных орбиталей (s, p, d, f) энергетические зоны кристалла разделяются на s-, p-, d-, f-зоны. Орбитали энергетической зоны заполняются электронами как обычные молекулярные орбитали с учетом принципа Паули и принципа минимума энергии, поэтому максимальное количество электронов в s-зоне равна 2NA , в p-зоне — 6NA , в d-зоне — 10NA и в f-зоне — 14NA .
Хотя зонная теория имеет описательный характер, она позволяет не только объяснить существование различных типов твердых тел (проводников, полупроводников, диэлектриков), но и понять оптические и магнитные свойства кристаллов. Однако важнейшее значение зонной теории заключается в том, что она позволяет регулировать многочисленные физические свойства твердых веществ и создавать на их основе новые материалы со специальными свойствами.
