Приведем пример эксперимента: в мерных цилиндрах находится пять бесцветных жидкостей, которые кажутся одинаковыми. Можно подумать, что в них налита вода. Но выпить какую-нибудь из них так же опасно, как стрелять в человека из винтовки, заряженной пятью патронами, из которых только один холостой. Если мы первую жидкость выльем на медную пластинку и зажжем спичку над ней, то…
- С первой ничего не произойдет
- Вторая жидкость воспламенится
- Третья — погасит пламя
- Четвертая разъест медную платинку
- А пятую мы не осмелимся пролить, так как она имеет высокую радиоактивность
Почему все пять жидкостей, внешне столь похожих, действуют, однако, совсем по-разному? Мы сможем ответить на этот вопрос после того, как узнаем, что такое химический элемент. Наши жидкости в действительности представляют собой простые соединения, и ни одно из них не содержит более трех или четырех элементов.
По химическому составу они намного проще дерева и камня, этих первых материалов, которые человек еще в глубокой древности научился обрабатывать для своих нужд.
В Бронзовом веке, наступившем намного позднее периода каменного молотка, человек начал непосредственно использовать элементы для изготовления разных предметов — от военного снаряжения и оружия и до безобидных булавок.
Во время Железного века человек овладевает мастерством извлечения металла из руд и перековывания его в различные полезные формы, например такие, как железный молоток.
В книгах, написанных в древние времена, рассказывается о том, что человек использовал золото, серебро, медь, железо, олово, углерод, свинец, серу и ртуть, однако, конечно, никто не предполагал, что все они являются химическими элементами.
В Средние века алхимики пытались делать разумные выводы из тех отрывочных и примитивных знаний по химии, которыми они располагали. Несмотря на незрелость и фантастичность многих их представлений, лучшие из алхимиков все же были учеными. Они хотели открыть основные кирпичи, из которых построены вещества, и с этой целью проводили опыты, в которых пытались их обнаружить.
Они считали такими основными элементами Огонь, Землю, Воздух и Воду. До сих пор их первая «система элементов» поражает нас. Она свидетельствует даже о том, что алхимикам были известны химические реакции. Например, дерево образует тепло при сгорании. Следовательно, считали они, сухое дерево состоит из Земли (золы) и Огня.
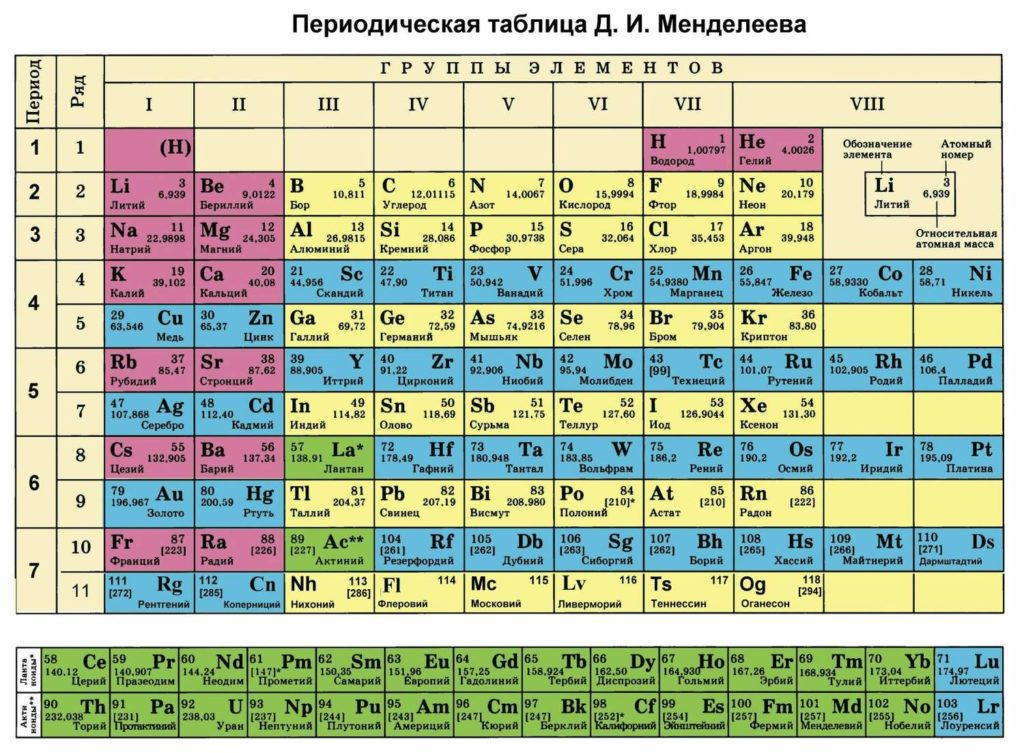
В настоящее время установлено, что все вещества на Земле и во Вселенной состоят из химических элементов. Мы хорошо знаем, что такое элемент, а наша периодическая система элементов совсем не похожа на систему алхимиков.
Теперь в этой таблице заключено большинство тайн, на разгадку которых алхимики тщетно тратили свои жизни. В наше время любой человек может получить обширную информацию, как только он научится читать периодическую систему. Она включает теперь свыше ста элементов вместо прежних четырех. Она характеризует вес и строение каждого элемента, и, только взглянув на нее, можно указать элементы, похожие друг на друга.
С помощью этой таблицы мы также можем описать огонь, землю, воздух и воду. Огонь представляет собой свет и тепло, образующиеся при соединении некоторых элементов с кислородом. Земля — это сложная комбинация многих десятков различных элементов. Воздух является смесью по крайней мере восьми элементов плюс одно соединение — углекислый газ. Вода — соединение, состоящее из двух элементов: кислорода и водорода.
Наша современная система элементов включает все элементы в порядке возрастания их атомных химического элемента для условным символом. Например, для первых восьми элементов приняты следующие сокращения: Н (водород), Не (гелий), Li (литий), Be (бериллий), В (бор), С (углерод),N (азот) и О (кислород).
Символы некоторых наиболее давно известных элементов получены от их первых названий, которыми больше не пользуются, наапример Hg для ртути и Ag (аргентум) для серебра. В периодической системе, в левом верхнем углу каждой клеточки указан атомный номер элемента. Так, для углерода он равен шести; это говорит о том, что атом углерода имеет 6 протонов в своем ядре, а следовательно, и 6 электронов.
Зная состав атома, мы тем самым знаем, как углерод будет соединяться с другими элементами. Число, находящееся внизу и для углерода имеющее значение немного большее 12, является атомным весом элемента. Для кислорода это число было принято равным 16. Таким образом, атом кислорода почти в шестнадцать раз тяжелее атома водорода.
Два этих числа характеризуют строение ядра элемента. Число протонов равно атомному номеру, т. е. для углерода — шести, а число нейтронов равно атомному весу минус атомный номер, т. е. для углерода 12-6 = 6. Для урана, атомный номер которого 92, а атомный вес 238, число протонов в ядре равно 92, а число нейтронов: 238—92=146.
Подробнее об этом в статье «Атомы химических элементов»
А теперь вернемся к нашему эксперименту, описанному в начале статьи. Пять чистых жидкостей, которые мы испытывали ранее, были простыми соединениями (точнее, последняя из них была раствором двух соединений). Кстати, все пять жидкостей состояли только из газообразных или из газообразных и твердых элементов. Вот эти жидкости:
- Вода (водород и кислород).
- Ацетон (водород, кислород и углерод) — та жидкость, которая воспламенялась.
- Четыреххлористый углерод (углерод и хлор) — та жидкость, которая гасила пламя.
- Азотная кислота (водород, кислород, азот) — та, которая химически реагировала с медной пластинкой.
- Раствор кобальта-60 — та, которая заставляла счетчик Гейгера трещать, как пулемет.